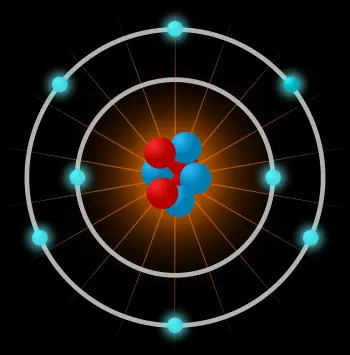
Um átomo é a menor unidade constituinte da matéria comum que possui as propriedades de um elemento químico. O átomo é composto por:
-
O núcleo atômico: formado por partículas subatômicas chamadas núcleons. Os núcleos podem ser nêutrons ou prótons.
-
Uma nuvem de elétrons: outro tipo de partícula subatômica que se move ao redor do núcleo.
A principal diferença entre prótons, nêutrons e elétrons é sua carga elétrica. Os elétrons têm carga elétrica negativa, os prótons têm carga positiva e os nêutrons são partículas com carga elétrica neutra.
Os átomos neutros têm o mesmo número de elétrons que prótons, uma vez que ambas as subpartículas têm a mesma carga elétrica.
Um átomo é composto de um núcleo central muito denso, com os núcleos próximos uns dos outros e elétrons que se movem ao redor do núcleo a uma distância relativamente grande.
Estrutura do núcleo do átomo
O núcleo atômico é a parte central do átomo que é composta de núcleos unidos por ligações muito fortes. Um nucleon pode ser um próton ou um nêutron.
Como os prótons têm carga elétrica positiva e os nêutrons com carga neutra, a tendência natural é a separação. As ligações que mantêm os núcleos unidos exercem uma força nuclear muito mais forte do que a força eletromagnética em curtas distâncias.
A força dessas ligações nucleares permite superar a repulsão elétrica entre os prótons.
Qual é o número de massa de um átomo?
O número de massa de um átomo é o número de núcleos em seu núcleo atômico, ou seja, a soma de prótons e nêutrons.
O volume do núcleo é aproximadamente proporcional ao número total de núcleons, o número de massa.
O que o número atômico representa?
O número atômico é o número de prótons que um átomo possui e é representado por Z.
Os átomos são classificados na tabela periódica dos elementos de acordo com o número atômico.
Isótopos: átomos com uma composição de núcleo diferente
Os átomos de um elemento químico devem ter o mesmo número de prótons, mas podem ter um número diferente de nêutrons. Os átomos do mesmo elemento com diferentes números de nêutrons são chamados de isótopos.
Os isótopos podem ser encontrados naturalmente, mas também podem ser manipulados. Por exemplo, o enriquecimento de urânio consiste em aumentar o número de nêutrons em um átomo de urânio para torná-lo mais instável e favorecer as reações de fissão.
O que é a nuvem de elétrons?
O elétron é uma partícula elementar estável com a menor carga negativa que existe na natureza. Essa carga é chamada de carga elementar, uma vez que qualquer carga elétrica separável é formada por um número inteiro delas.
Os elétrons possuem carga elétrica negativa, portanto são atraídos pelos prótons, de sinal positivo no átomo, através da força eletromagnética. Essa força aumenta reduzindo a distância entre o elétron e o núcleo.
A existência do elétron foi descoberta por JJ Thomson. A partir deste momento já apareceu em todos os modelos atômicos desenvolvidos no futuro.
Orbitais atômicos: a probabilidade de encontrar um elétron em um ponto
Os elétrons tendem a formar um certo tipo de onda estacionária em torno do núcleo atômico. Cada uma dessas ondas é caracterizada por um orbital atômico, uma função matemática que descreve a probabilidade de encontrar o elétron em cada ponto do espaço.
A nuvem de elétrons é a região ocupada por essas ondas, visualizada como uma densidade de carga negativa ao redor do núcleo.
Cada orbital corresponde a um possível valor de energia para elétrons. No entanto, um elétron pode saltar para um nível superior ou inferior, capturando ou emitindo energia.
O conceito de orbital atômico foi introduzido pela primeira vez no modelo atômico de Schrödinger.
Qual a importância da composição de um átomo para a energia nuclear?
A base de tudo o que se relaciona com a energia nuclear está no núcleo do átomo, já que a tecnologia nuclear se baseia no aproveitamento da energia interna contida nos átomos.
A energia nuclear é obtida da divisão do núcleo de um átomo (fissão nuclear) ou da fusão de dois núcleos atômicos (fusão nuclear).
Quando isso acontece e a estrutura do átomo muda, uma grande quantidade de energia térmica é liberada.
Reações nucleares: fissão e fusão de átomos
O núcleo atômico pode ser alterado por processos muito energéticos que podem causar uma mudança na estrutura do átomo. Os núcleos instáveis de urânio e plutônio podem sofrer decaimentos que podem alterar o número de prótons e nêutrons pela emissão de radiação.
Um núcleo pesado pode fissão em núcleos mais leves em uma reação nuclear ou espontaneamente. Por meio de uma quantidade de energia suficiente, dois ou mais núcleos podem se fundir em um mais pesado, neste caso, seria uma reação de fusão nuclear.
Elementos químicos que possuem um número atômico baixo, núcleos com diferentes números de prótons e nêutrons tendem a se desintegrar em núcleos com proporções mais semelhantes. No entanto, os elementos mais pesados precisam de uma proporção maior de nêutrons para estabilizar o núcleo.
