Os átomos, os blocos de construção fundamentais da matéria, são compostos de prótons, nêutrons e elétrons. No entanto, existem diferentes versões do mesmo elemento químico. Essas variantes, conhecidas como isótopos, abrem a porta para um mundo de diversidade atômica e propriedades únicas.
Neste artigo, exploraremos alguns exemplos notáveis. Desde isótopos usados na datação de fósseis e rochas antigas até aqueles que nos fornecem energia em reatores nucleares, descobriremos as características e aplicações de alguns desses elementos atômicos únicos.
Os isótopos de urânio são particularmente relevantes porque são usados como combustível em usinas nucleares que usam reatores de fissão. Deutério e trítio, mencionados abaixo, são os isótopos que estão sendo trabalhados em reatores de fusão nuclear.
Isótopos de urânio e plutônio: Energia nuclear e armas
Urânio-235 (²³⁵U)
O urânio-235 é o isótopo físsil mais importante do urânio e um dos poucos materiais capazes de sustentar uma reação em cadeia. Sua capacidade de se dividir em núcleos menores quando bombardeado por nêutrons o torna um elemento-chave para a geração de energia nuclear e a fabricação de armas nucleares.
Em reatores nucleares, o urânio-235 enriquecido é usado como combustível, gerando grandes quantidades de calor por meio da fissão nuclear controlada. Esse calor é usado para aquecer água e produzir vapor, que por sua vez aciona turbinas que geram eletricidade. Além disso, o urânio-235 é usado na produção de isótopos radioativos usados na medicina, como o tecnécio-99m, que é usado em gamagrafia para o diagnóstico de doenças.
Devido ao seu potencial uso em armas nucleares, o urânio-235 está sujeito a regulamentações rigorosas e medidas de controle internacional para impedir sua proliferação.
Urânio-238 (²³⁸U)
É o isótopo mais abundante de urânio, representando aproximadamente 99,3% do urânio natural. Embora não seja diretamente físsil, ele pode ser transformado em plutônio-239 pelo bombardeio de nêutrons em reatores nucleares, tornando-o um material estratégico para a produção de combustível nuclear.
Além de seu uso em reatores, o urânio-238 é usado na datação radiométrica de rochas e minerais usando o método urânio-chumbo, permitindo determinar a idade de formações geológicas. Ele também é usado na fabricação de blindagem de alta densidade para proteção contra radiação e em certos tratamentos de medicina nuclear, como a tomografia por emissão de pósitrons (PET).
Plutônio-239 (²³⁹Pu)
Plutônio-239 é um isótopo altamente radioativo e físsil usado em armas nucleares e reatores nucleares avançados. Nas bombas atômicas, sua capacidade de gerar reações em cadeia descontroladas foi explorada em dispositivos altamente destrutivos.
No reino pacífico, o plutônio-239 é usado como fonte de energia em reatores de fissão e em geradores de radioisótopos usados em sondas espaciais, como as missões Voyager e Curiosity, onde sua decomposição radioativa fornece energia elétrica em ambientes onde a energia solar não é viável.
Isótopos de hidrogênio: Chaves para a fusão nuclear e a ciência
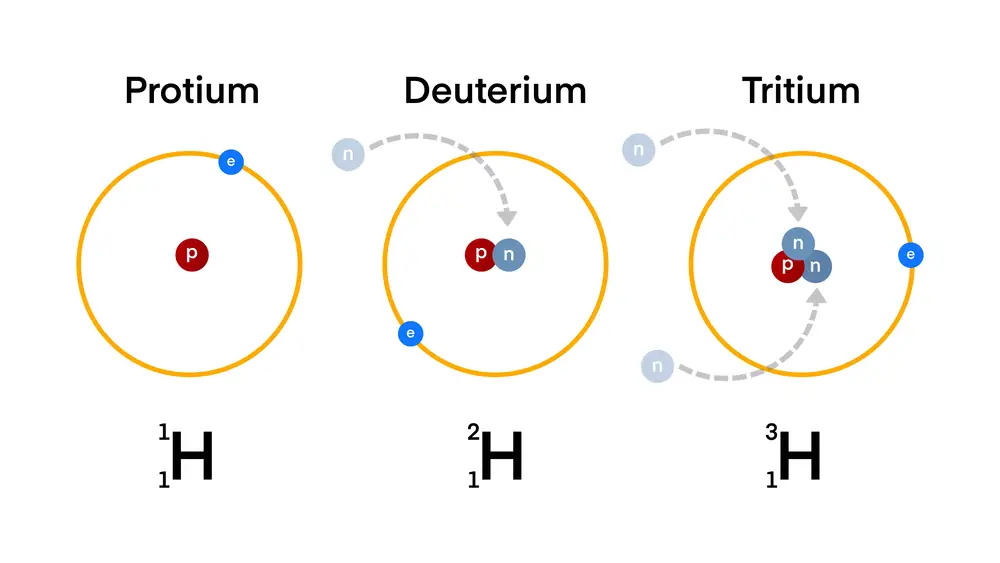
Hidrogênio-2 (²H) ou deutério
O deutério é um isótopo estável do hidrogênio com um nêutron extra em seu núcleo, o que o torna mais pesado que o hidrogênio comum. Sua aplicação mais relevante é na produção de água pesada (D₂O), utilizada como moderador de nêutrons em certos tipos de reatores nucleares.
Ele também desempenha um papel crucial na pesquisa de fusão nuclear, onde a possibilidade de combinar deutério e trítio para gerar energia limpa e sustentável está sendo estudada. Além disso, em química e biomedicina, o deutério é usado em estudos de ressonância magnética nuclear (RMN) para analisar a estrutura de moléculas.
Hidrogênio-3 (³H) ou trítio
O trítio é um isótopo radioativo do hidrogênio usado em reatores experimentais de fusão nuclear, onde sua combinação com o deutério pode fornecer uma fonte quase ilimitada de energia no futuro. Também é usado em dispositivos de iluminação radioluminescentes, como placas de emergência e relógios, devido à sua capacidade de emitir luz sem a necessidade de energia externa.
Na pesquisa científica, o trítio é usado como traçador em estudos ambientais e biológicos, permitindo a análise do movimento da água em ecossistemas ou processos metabólicos em organismos vivos.
Hidrogênio-1 (¹H) ou prótio
O prótio é o isótopo mais comum do hidrogênio, respondendo por aproximadamente 99,98% de todo o hidrogênio presente na Terra. Seu núcleo consiste em um único próton sem nêutrons, tornando-o o isótopo mais leve de todos os elementos.
Este isótopo é essencial em vários processos naturais e tecnológicos. Na indústria, é usado na produção de gás hidrogênio (H₂), que é usado como combustível em células de combustível para gerar eletricidade de forma limpa. Também é essencial na síntese de amônia através do processo Haber-Bosch, essencial para a produção de fertilizantes.
No campo da astrofísica, o prótio é o principal componente do Sol e de outras estrelas, onde participa de reações de fusão nuclear que geram a energia que alimenta nosso sistema solar. Além disso, é amplamente utilizado em espectroscopia de ressonância magnética nuclear (RMN), uma técnica fundamental para a análise estrutural de moléculas em química e biologia.
Isótopos usados em datação e diagnóstico médico
Carbono-14 (¹⁴C)
Este isótopo radioativo de carbono é essencial na datação por radiocarbono, uma técnica usada para estimar a idade de vestígios arqueológicos e fósseis de origem orgânica. Sua presença nos seres vivos cessa quando eles morrem, e sua desintegração nos permite calcular quanto tempo se passou desde então. Essa técnica tem sido fundamental na arqueologia e na paleontologia, ajudando a entender a história da humanidade e do planeta.
Iodo-131 (¹³¹I)
O iodo-131 é um isótopo radioativo usado em medicina nuclear para o tratamento de doenças da tireoide, como hipertireoidismo e câncer de tireoide. Sua radiação beta destrói células anormais da tireoide sem a necessidade de procedimentos invasivos, o que a torna uma opção terapêutica eficaz. Também é usado no diagnóstico da função tireoidiana por meio de gamagrafia.
Tecnecio-99m (⁹⁹ᵐTc)
É um dos isótopos mais utilizados em medicina nuclear devido à sua curta meia-vida e à sua capacidade de emitir radiação gama sem afetar significativamente o paciente. É usado em gamagrafia para visualizar órgãos e tecidos, auxiliando na detecção de doenças cardiovasculares, ósseas e oncológicas. Seu uso revolucionou o diagnóstico por imagem, permitindo avaliações precisas com impacto mínimo no corpo.
Aplicações industriais e de radioterapia
Cobalto-60 (⁶⁰Co)
Cobalto-60 é um isótopo radioativo com aplicações em radioterapia contra câncer. Suas poderosas emissões de raios gama atingem as células cancerígenas, danificando seu DNA e impedindo sua proliferação. Também é utilizado na esterilização de equipamentos médicos e na irradiação de alimentos para eliminar microrganismos sem afetar sua qualidade nutricional.