A Química é uma ciência baseada na organização dos elementos químicos da tabela periódica, ferramenta essencial para a compreensão e previsão do comportamento de átomos e moléculas.
Ao longo da história, vários cientistas contribuíram para o desenvolvimento da tabela periódica, e uma das primeiras tentativas de organizar os elementos foi a lei das oitavas.
Origens históricas
 A lei das oitavas é um conceito que se originou em meados do século XIX, quando o químico britânico John Newlands notou uma tendência nas propriedades químicas dos elementos.
A lei das oitavas é um conceito que se originou em meados do século XIX, quando o químico britânico John Newlands notou uma tendência nas propriedades químicas dos elementos.
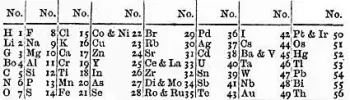
Em 1864, Newlands propôs sua ideia em um artigo intitulado “Sobre a Lei das Oitavas”. Neste trabalho, Newlands observou que quando os elementos são organizados em ordem crescente de massa atômica, as propriedades químicas parecem se repetir a cada oito elementos.
Essa repetição lembra a repetição de notas musicais em uma oitava musical, daí o nome “lei das oitavas”.
Limitações da lei das oitavas
Embora a lei das oitavas tenha sido um passo importante para a organização dos elementos, ela tinha limitações significativas.
A principal limitação era que só funcionava para alguns dos elementos conhecidos na época. Por outras palavras, a lei não foi aplicada de forma consistente a todos os elementos. Newlands só poderia aplicar sua lei aos primeiros 56 elementos da tabela periódica e, depois disso, a repetição das propriedades químicas não era mais evidente.
Além disso, Newlands também cometeu erros na organização de alguns elementos. Por exemplo, ele colocou ferro e cobalto na mesma coluna, embora suas propriedades químicas sejam visivelmente diferentes.
Tabela periódica de Mendeleev: superando a lei das oitavas
Apesar das suas limitações, a lei das oitavas lançou as bases para a criação posterior da tabela periódica moderna. O químico russo Dmitri Mendeleev, contemporâneo de Newlands, estava trabalhando em uma organização semelhante dos elementos e desenvolveu sua própria versão da tabela periódica em 1869.
A contribuição mais importante de Mendeleev foi reconhecer que a organização dos elementos devia basear-se nas suas massas atómicas, mas também devia ter em conta as suas propriedades químicas e a periodicidade dessas propriedades.
Organização da tabela Mendeleev
Mendeleev organizou os elementos com base em sua massa atômica crescente, mas deixou espaços vazios na tabela periódica onde ele acreditava que deveriam estar os elementos desconhecidos na época.
O que foi surpreendente foi que as propriedades químicas dos elementos desconhecidos se ajustavam perfeitamente às previsões de Mendeleev quando foram posteriormente descobertos.
Osolescência da lei das oitavas
O sucesso da tabela periódica de Mendeleev e sua capacidade de prever as propriedades de elementos ainda não descobertos tornaram a lei das oitavas de Newlands obsoleta e considerada insuficiente para explicar a organização dos elementos.
A tabela periódica moderna e a organização dos elementos
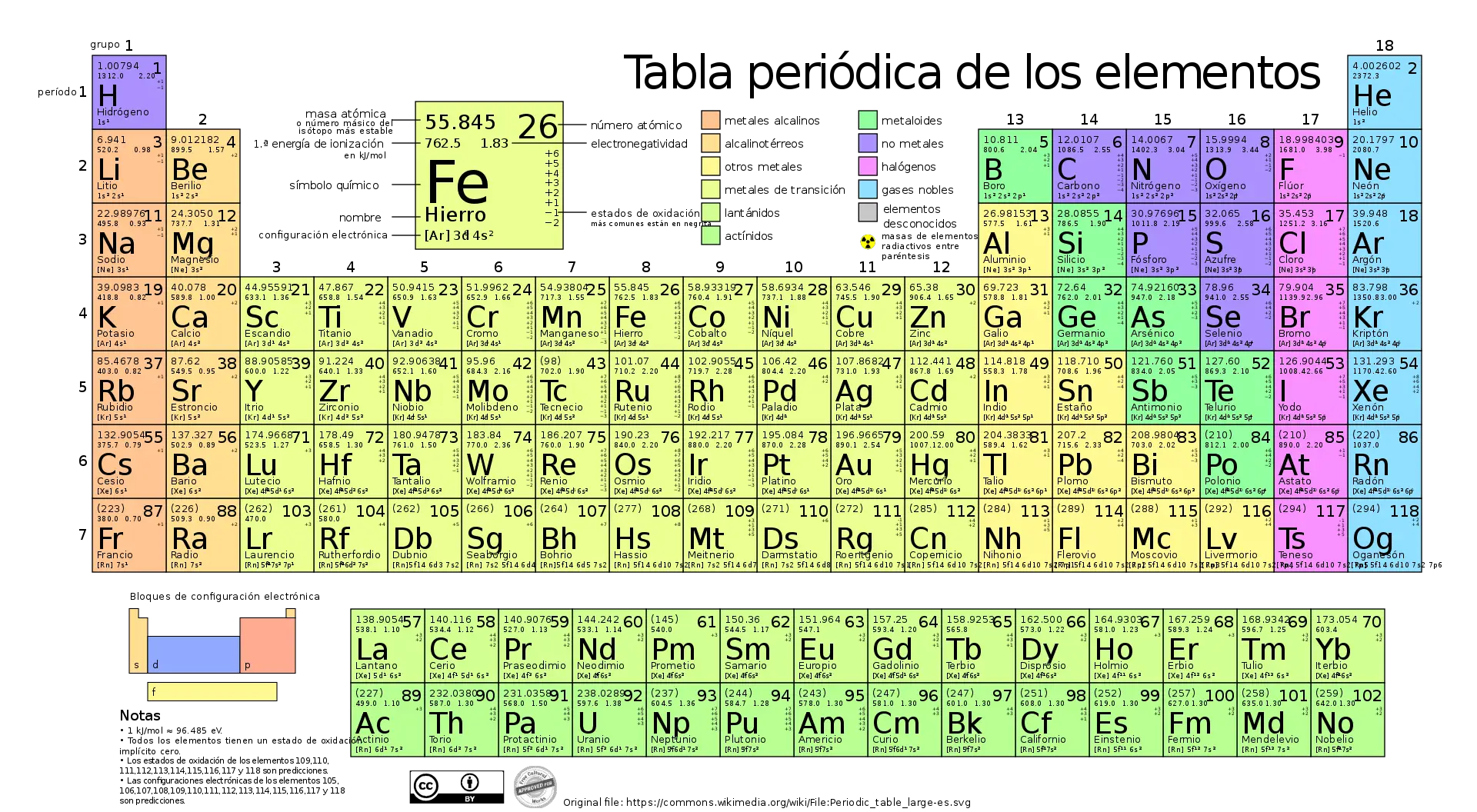 A tabela periódica moderna baseia-se na estrutura e organização propostas por Mendeleev, mas evoluiu ao longo do tempo à medida que mais elementos foram descobertos e progressos foram feitos na compreensão da estrutura atómica e das propriedades químicas.
A tabela periódica moderna baseia-se na estrutura e organização propostas por Mendeleev, mas evoluiu ao longo do tempo à medida que mais elementos foram descobertos e progressos foram feitos na compreensão da estrutura atómica e das propriedades químicas.
Na tabela periódica atual, os elementos são organizados com base no seu número atômico, que é o número de prótons no núcleo de um átomo. Isto resulta em uma organização que mostra claramente a periodicidade das propriedades químicas dos elementos.
As linhas horizontais, chamadas de períodos, representam níveis de energia em que os elétrons podem ser encontrados, e as colunas verticais, chamadas de grupos, possuem elementos com propriedades químicas semelhantes devido à sua configuração eletrônica semelhante.
Conclusões
A lei das oitavas foi uma tentativa antiga e valiosa de organizar os elementos químicos, mas tinha limitações importantes e não conseguia explicar adequadamente a organização de todos os elementos.
Foi a tabela periódica de Mendeleev que finalmente superou essas limitações e se tornou a ferramenta essencial que conhecemos hoje.
A organização dos elementos na tabela periódica moderna é baseada no número atômico e reflete com precisão a periodicidade das propriedades químicas dos elementos, o que tem sido fundamental para o avanço da química e para a compreensão da matéria no nível atômico.
Em resumo, a lei das oitavas foi um passo importante neste caminho, mas foi apenas o início de um processo contínuo de descoberta e organização na química.
