O cálcio, elemento químico essencial à vida, é conhecido pelo seu papel na saúde dos ossos e dentes. No entanto, a relevância do cálcio vai além da biologia humana e estende-se a uma vasta gama de campos científicos.
A massa atômica do cálcio é um conceito físico e químico que se refere à massa média de todos os isótopos de cálcio encontrados na natureza, ponderada pela sua abundância relativa.
A massa atômica é expressa em unidades de massa atômica unificada (uma) ou daltons (Da), e para o cálcio, sua massa atômica média é de aproximadamente 40.078 u.
Cálculo da massa atômica do cálcio
A massa atômica do cálcio é calculada levando-se em consideração a abundância relativa de seus isótopos naturais.
O cálcio possui vários isótopos, sendo o mais abundante o cálcio-40 (Ca-40), que representa aproximadamente 96% de todo o cálcio natural. Além disso, o cálcio-44 (Ca-44) é outro isótopo comum, constituindo aproximadamente 2,1% do cálcio natural. Outros isótopos de cálcio, como Ca-42 e Ca-48, são menos abundantes e têm um efeito menor na massa atômica média.
O cálculo da massa atômica é feito multiplicando a massa de cada isótopo pela sua abundância relativa e somando os resultados. No caso do cálcio, isso resulta em uma massa atômica média de cerca de 40.078 u.
Tabela com as massas atômicas dos isótopos de cálcio
A tabela a seguir mostra a massa atômica de cada isótopo de cálcio e a porcentagem de sua composição isotópica.
|
Isótopo |
Massa atômica (Da) |
Abundância isotópica (fração de quantidade) |
|
40Ca _ |
39.962 5909 (2) |
96,941% (156) |
|
42Ca _ |
41.958 618 (1) |
0,647% (23) |
|
43Ca _ |
42.958 766 (2) |
0,135% (10) |
|
44Ca _ |
43.955 482 (2) |
2,086% (110) |
|
46Ca _ |
45.953 69 (2) |
0,004% (3) |
|
48 Ca |
47.952 5229 (6) |
0,187% (21) |
Propriedades e características do cálcio
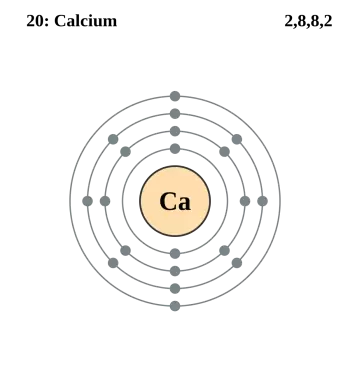
 O cálcio (Ca) é um elemento químico da tabela periódica com número atômico 20. Esse número atômico indica que um átomo de cálcio possui 20 prótons em seu núcleo e, consequentemente, 20 elétrons orbitando ao seu redor.
O cálcio (Ca) é um elemento químico da tabela periódica com número atômico 20. Esse número atômico indica que um átomo de cálcio possui 20 prótons em seu núcleo e, consequentemente, 20 elétrons orbitando ao seu redor.
A forma pura do cálcio é um metal alcalino-terroso branco prateado, conhecido por sua reatividade e caráter suave. Foi em 1808 que Sir Humphry Davy conseguiu isolá-lo pela primeira vez na sua forma pura.
Devido à sua alta atividade química, o cálcio não é encontrado livremente na natureza. Porém, é possível obter cálcio metálico puro através do processo de eletrólise de um fundido.
O cálcio é o quinto elemento mais abundante na Terra, depois do oxigênio, silício, alumínio e ferro. Além disso, é um elemento encontrado em grandes quantidades na água do mar, com concentração aproximada de 400 mg/l. Na verdade, constitui cerca de 3,38% da massa total da crosta terrestre.
Este elemento químico pertence ao grupo dos metais alcalino-terrosos e compartilha sua alta atividade química com outros membros deste grupo da tabela periódica. Apesar da sua atividade, existem outros metais alcalinos que são ainda mais reativos.
Na natureza, o cálcio é comumente encontrado associado ao dióxido de carbono, oxigênio e umidade presentes no ar, o que contribui para sua presença em diversas formas e compostos em nosso meio ambiente.
Importância da massa atômica do cálcio
A massa atômica do cálcio é um conceito de grande importância na química, física e biologia. Esta magnitude não só é essencial para a compreensão das propriedades e comportamento do próprio cálcio, mas também tem inúmeras aplicações em diferentes campos científicos.
- Em química, a massa atômica do cálcio é usada para calcular a massa molar de compostos contendo cálcio. A massa molar é crucial para a formulação de substâncias e a compreensão das proporções nas reações químicas. Por exemplo, no carbonato de cálcio (CaCO₃), a massa molar é calculada somando a massa de cálcio, carbono e oxigênio, o que permite determinar a quantidade de substância presente em uma amostra.
- Na física nuclear, a massa atômica do cálcio é essencial para calcular a energia de ligação dos núcleos atômicos. A energia de ligação é necessária para compreender processos como a fissão e a fusão nuclear, que são fundamentais tanto nas aplicações energéticas como na compreensão da estrutura da matéria.
- Na astrofísica, a massa atômica do cálcio é relevante na nucleossíntese estelar, onde os elementos mais pesados são formados a partir de elementos mais leves dentro das estrelas. O cálcio é produzido neste processo, e sua massa atômica ajuda a explicar a abundância de cálcio no universo e como os elementos são formados.
- Na biologia, o cálcio é essencial para a saúde dos seres vivos, incluindo os humanos. A massa atômica do cálcio é fundamental para calcular a quantidade de cálcio necessária na dieta e compreender seu papel na formação óssea, na transmissão de sinais nervosos e em muitas outras funções biológicas.
